摘要

关键词
- 头颈癌 (Head and Neck Cancer)
- 器官风险区 (Organs-at-Risk, OARs)
- 深度学习 (Deep Learning)
- 辐射治疗 (Radiotherapy)
- 神经网络 (Neural Network)
研究背景
头颈部肿瘤的放射治疗对正常器官的精确保护至关重要,传统的手动描绘方法耗时且受医生经验限制,导致大部分机构仅绘制少量关键器官区域,这可能遗漏其他重要器官的剂量分布信息。近年来,深度学习方法逐步应用于自动分割领域,但大多数现有方法仅支持20个左右的器官分割。本研究旨在开发一种高效且全面的分割系统,以实现更广泛的器官覆盖及更精确的临床应用。
创新点
- 提出了分层学习框架,将器官分为锚定级、中级、小型复杂级别进行分割。
- 使用神经网络架构搜索(NAS)优化了不同器官类别的网络结构。
- 在多机构大规模数据上验证了模型的泛化性能。
- 显著减少了医生手动修订分割结果的时间。
研究内容
SOARS系统采用了分层处理和NAS优化架构,将器官分为锚定级、中级及小型复杂器官,通过三个不同分支分别处理。模型训练基于来自6家机构的1503例患者数据,内部和外部测试集中覆盖了42个器官。实验表明,SOARS在分割准确性、临床适用性和辐射剂量评估方面优于现有方法,尤其在小型复杂器官的分割中表现突出。

我们总共收集了1503例头颈部(HN)癌症患者来开发和评估所提出的分层器官危险分割(SOARS)的性能。
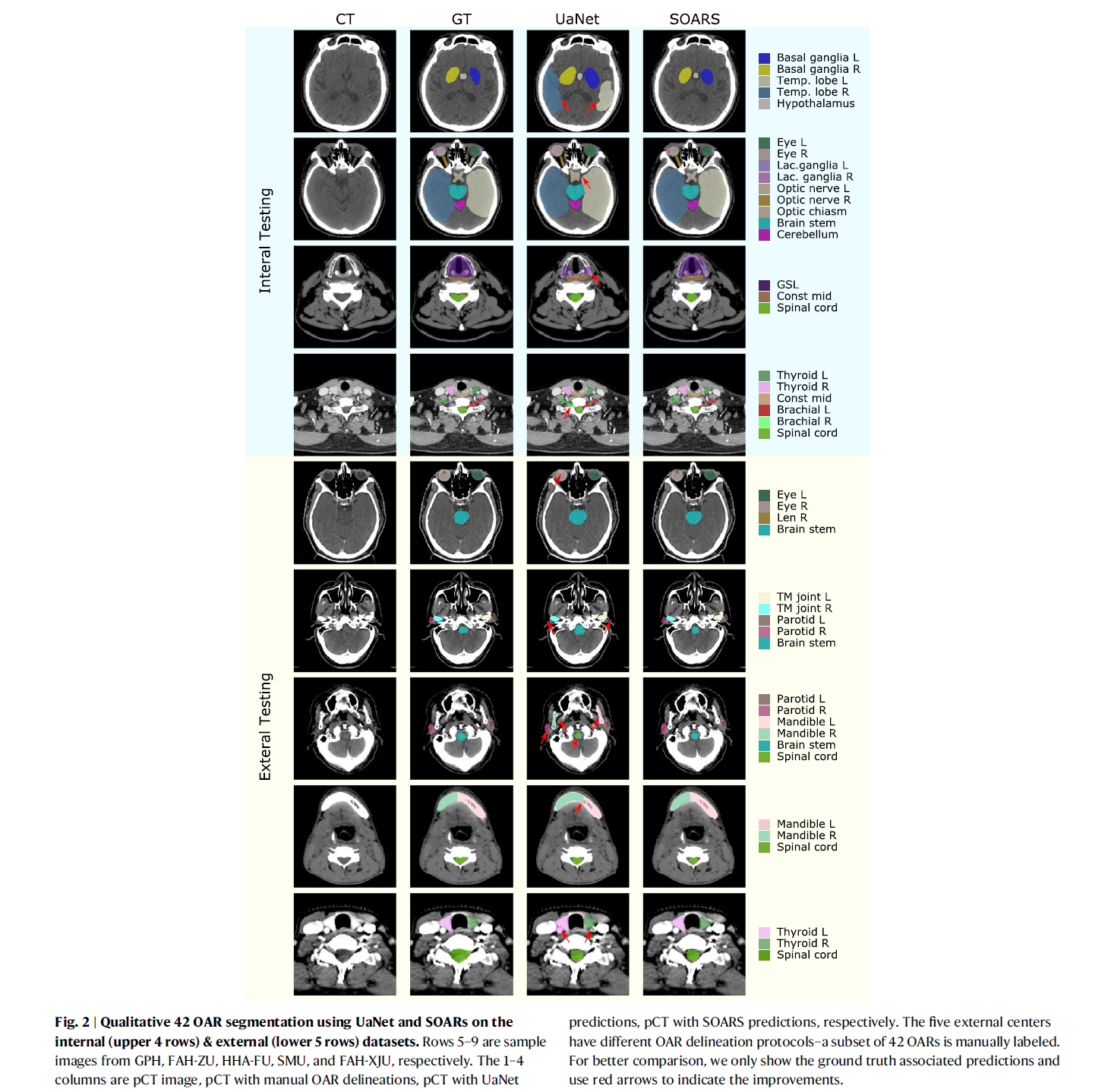
内部测试数据集中四个样本影像的锚定、中层及小而难分器官分割的定性对比。红色箭头指向代表SOARS比对比方法(如UaNet)更好的分割结果。多中心外部数据集中的一些典型样本,并通过人工标注、UaNet预测和SOARS预测进行对比。
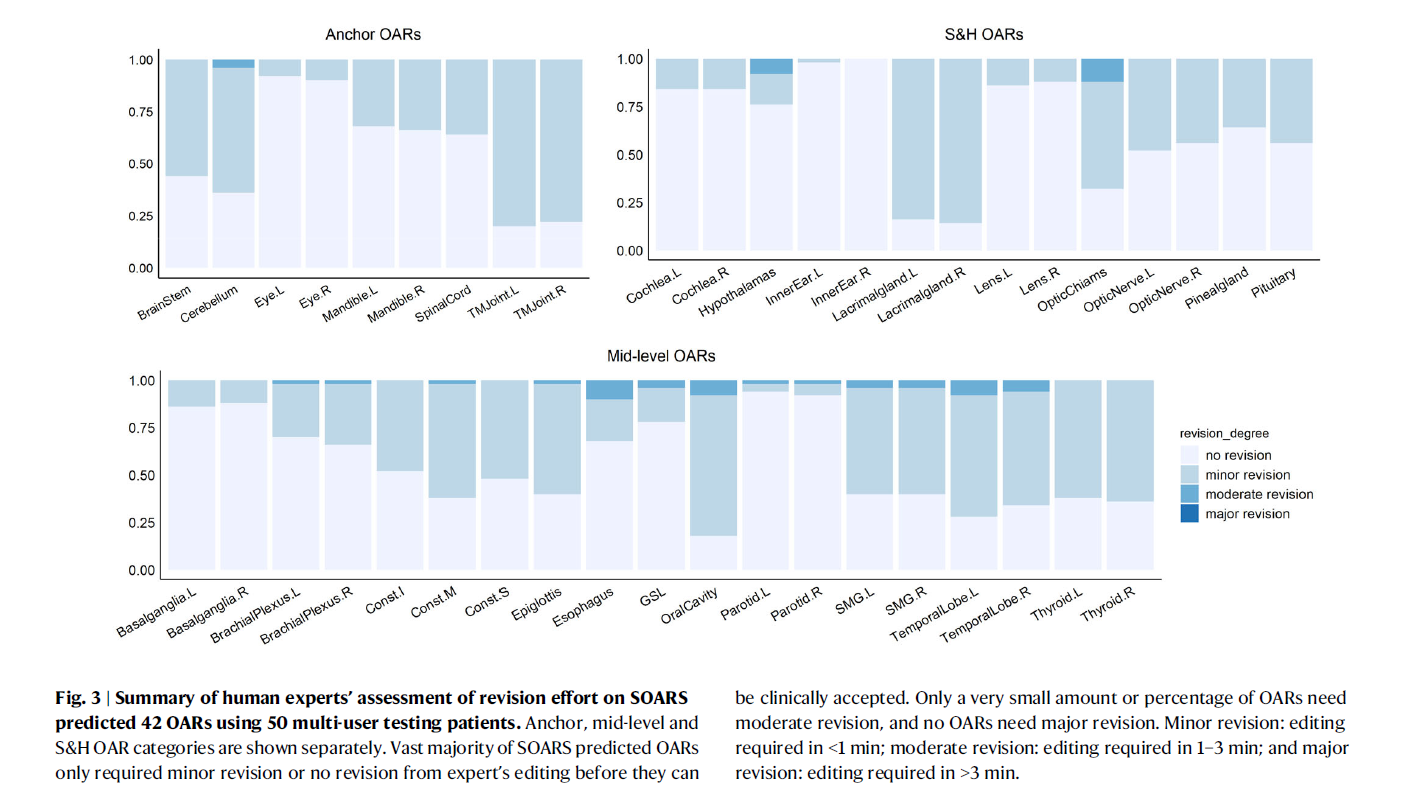
柱状图显示了锚定层、中层及小而难分器官类别的修订情况,绝大多数SOARS预测仅需轻微修改或无需修改即可被临床接受。轻微修改定义为<1分钟;中等修改为1-3分钟;无严重修改的需要。
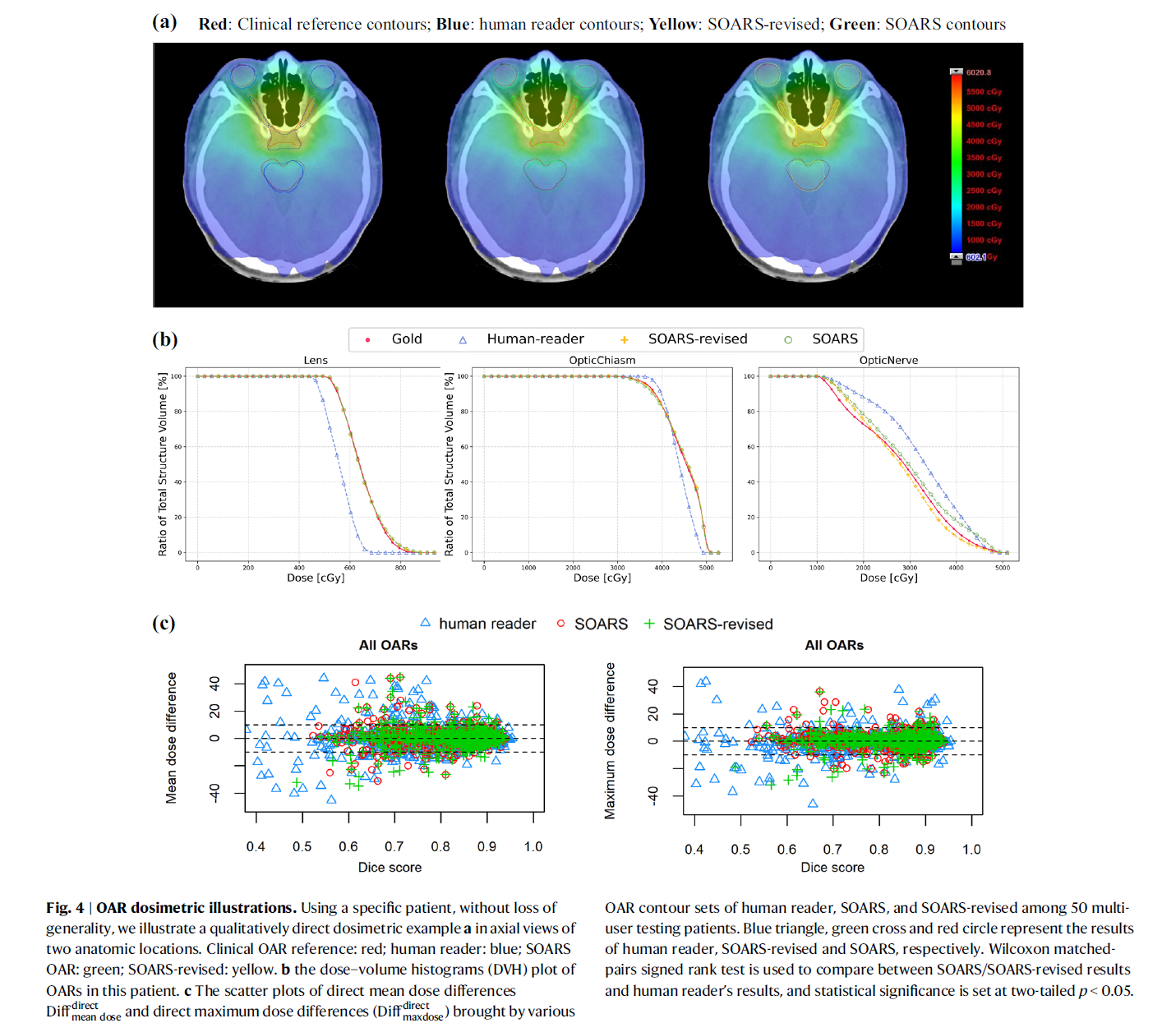
(a) 显示了某患者的直接剂量学对比示例,分别在两个解剖位置中展示不同OAR轮廓对剂量分布的影响。(b) 显示剂量-体积直方图(DVH)。(c) 散点图展示了不同轮廓集对直接剂量差异的影响,包括SOARS、SOARS修订版以及人工标注。
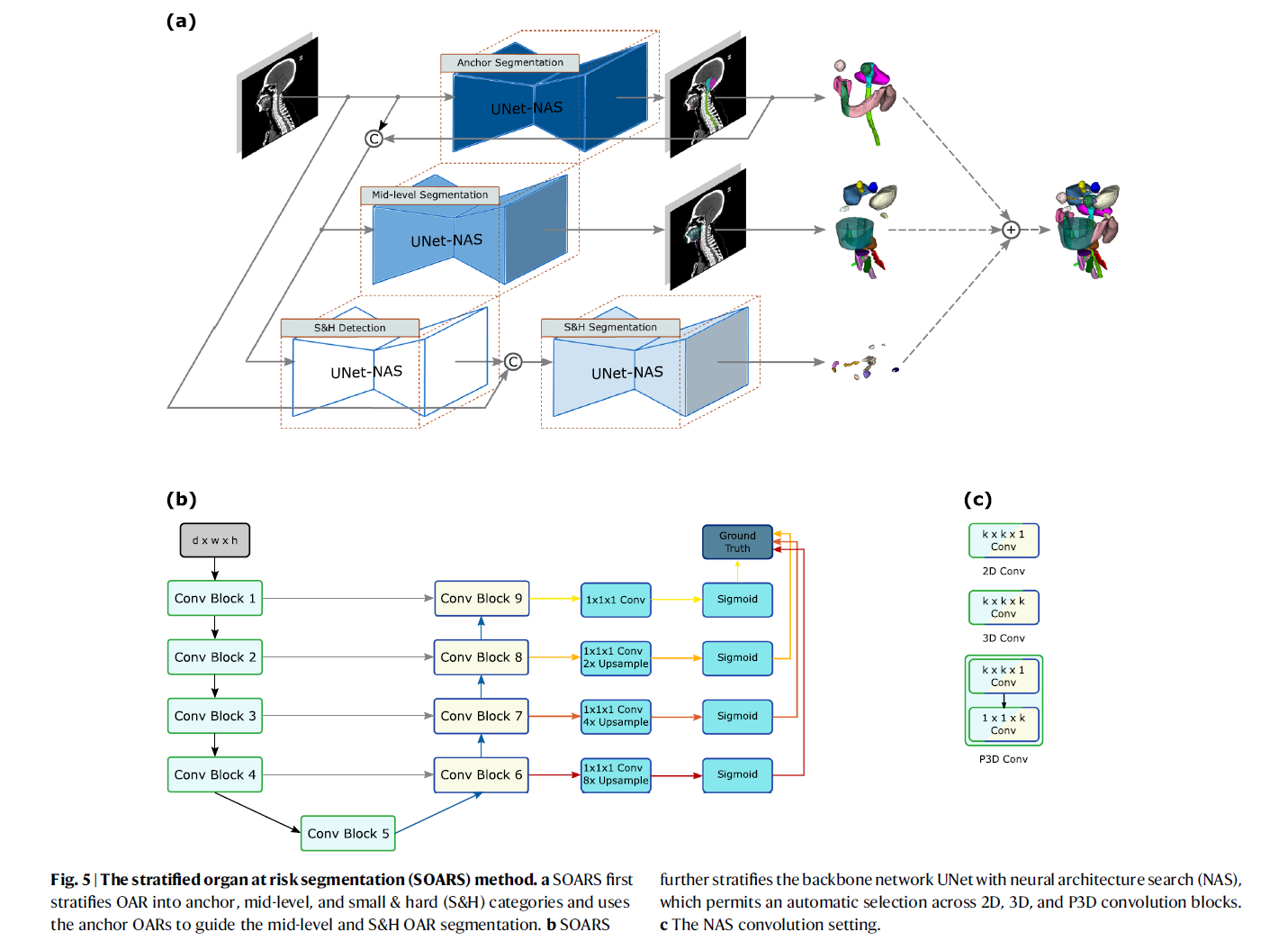
(a) SOARS将OAR分层为锚定、中层及小而难分类别,并利用锚定层指导其他类别的分割。(b) 使用NAS优化的分割网络骨干架构。(c) 展示了NAS卷积设置。
结论与展望
SOARS通过分层学习和NAS优化显著提高了头颈部42个器官的分割精度和效率,大大减少了医生的工作量。未来,SOARS有望扩展至其他解剖区域,进一步支持多机构放疗剂量学研究及改善患者治疗质量。
论文直达
原文标题:Comprehensive and Clinically Accurate Head and Neck Cancer Organs-at-Risk Delineation on a Multi-Institutional Study
Nat. Commun. 2022, 13, 6137.
点击以下链接阅读原文:

