摘要

关键词
- 反双极性 (Antiambipolarity)
- 有机电化学神经元 (Organic Electrochemical Neuron, c-OECN)
- 混合导电聚合物 (Mixed Ion–Electron Conducting Polymers)
- 离子调控 (Ion Tuning)
- 神经形态传感 (Neuromorphic Sensing)
- 生物整合 (Biointegration)
- 生物信号调制 (Biochemical Signal Modulation)
研究背景
生物神经元依赖膜电位尖峰进行信息传递,这种过程由细胞膜内的离子通道(如钠通道和钾通道)动态控制。传统的人工神经元通常基于硅基电路,尽管可以模拟部分神经功能,但其制造复杂且缺乏生物兼容性和离子/化学信号调控能力。有机电化学晶体管(OECT)因其低工作电压、生物相容性和高离子灵敏度,为构建类似生物的电化学神经元提供了可能性。本研究利用反双极行为实现了生物真实的尖峰动态,并首次将其应用于生物体内的神经刺激。
创新点
- 开发了基于反双极特性的离子调控机制,模拟了钠通道的激活和失活特性。
- 实现了接近100 Hz的生物真实尖峰频率和多种神经行为的模拟。
- 展示了通过离子、神经递质和氨基酸调控尖峰行为的能力。
- 成功将c-OECN与小鼠迷走神经整合,用于心率调节。
研究内容
本研究利用含刚性梯形结构的聚合物(BBL)构建了具有反双极特性的OECT,用于模拟生物神经元中的钠钾离子通道动态。实验表明,通过调节电路中的膜电容和通道阻值,可以实现从5 Hz到100 Hz的尖峰频率。通过外加钙离子、神经递质和氨基酸等生物分子,进一步调节了尖峰行为的模式。研究还验证了c-OECN在体内生物信号感知和神经刺激的可行性,例如通过调节钠离子浓度实现对小鼠迷走神经的控制,从而降低心率。这一整合展示了c-OECN在生物医学领域的巨大潜力。
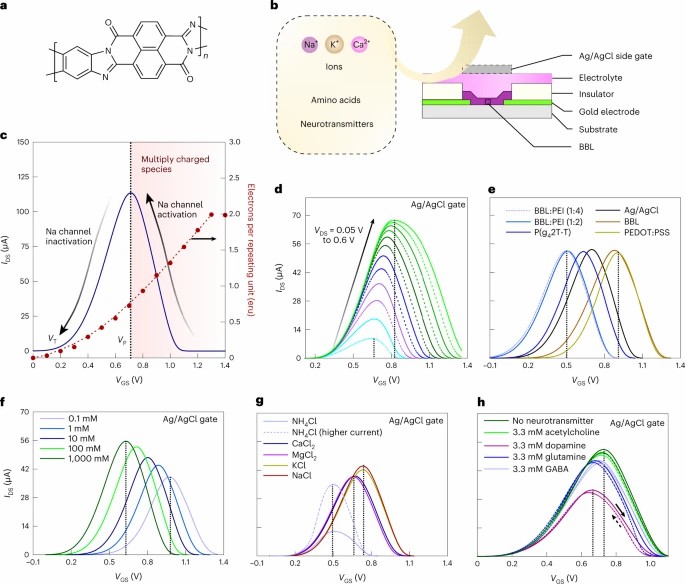
(a) BBL 的分子结构。 (b) OECT 器件的结构示意图。 (c) BBL 的反双极行为模拟了神经元中钠通道的激活和失活状态。 (d–h) 通过电学和化学手段调控反双极行为,显示漏极电压 (\(V_{\text{DS}}\)) 依赖性 (d)、不同栅极材料 (e)、离子浓度 (f)、离子类型 (g) 和不同氨基酸/神经递质 (h) 的影响。用于比较的 OECT 具有 \(W/L = 40 \, \mu \text{m}/6 \, \mu \text{m}\) 且 BBL 厚度为 20 nm,除高电流 NH\(_4\)Cl 器件外,其通道宽度为 \(W/L = 400 \, \mu \text{m}/6 \, \mu \text{m}\)。比较各种离子类型的浓度为 100 mM,神经递质和氨基酸研究在 100 mM NaCl 电解质中进行。d–h 中的竖直虚线表示漏极电流峰值 (\(V_P\)) 对应的栅极电压,h 中实线和虚线分别表示正向和反向扫描。
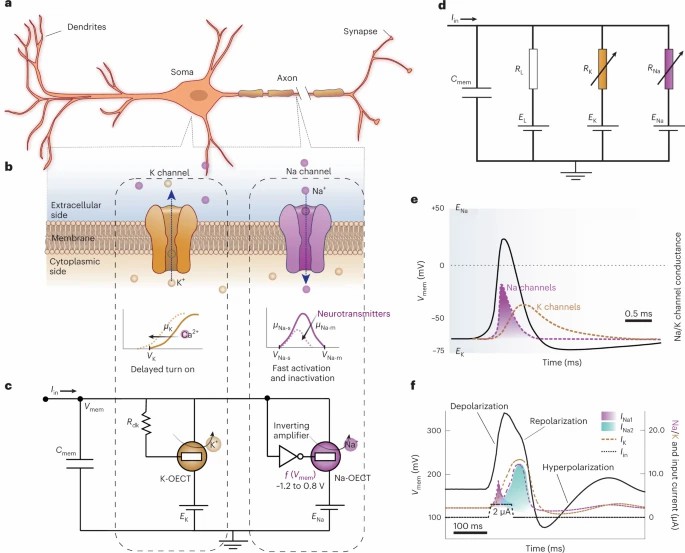
(a–c) 比较生物神经元 (a) 显示的 Na\(^+\) 和 K\(^+\) 通道 (b) 与 c-OECN 电路中 Na\(^+\)- 和 K\(^+\)- 基 OECT 的模拟 (c) 及其对 Ca\(^{2+}\) 和神经递质的调控。 (d) Hodgkin-Huxley 神经元模型的电路表示。 (e, f) 比较 Hodgkin 和 Huxley 研究的鱿鱼轴突动作电位 (e) 与 c-OECN 动作电位 (f)。图中 \(C_{\text{mem}}\) 表示膜电容,\(V_{\text{mem}}\) 表示膜电压,\(I_{\text{in}}\) 表示输入电流,\(R_{\text{dk}}\) 表示引起延迟的电阻。\(E_L (R_L), E_K (R_K), E_{\text{Na}} (R_{\text{Na}})\) 分别表示 HH 模型中的泄漏、钾和钠电池 (电阻)。\(V_K\) 和 \(\mu_K\) 表示 K-OECT 的阈值电压和迁移率,\(V_{\text{Na-s}} (\mu_{\text{Na-s}})\) 和 \(V_{\text{Na-m}} (\mu_{\text{Na-m}})\) 表示 Na-OECT 反双极传输曲线低电压侧和高电压侧的阈值电压 (迁移率)。\(I_{\text{Na}}\) 和 \(I_K\) 分别是钠和钾电流。
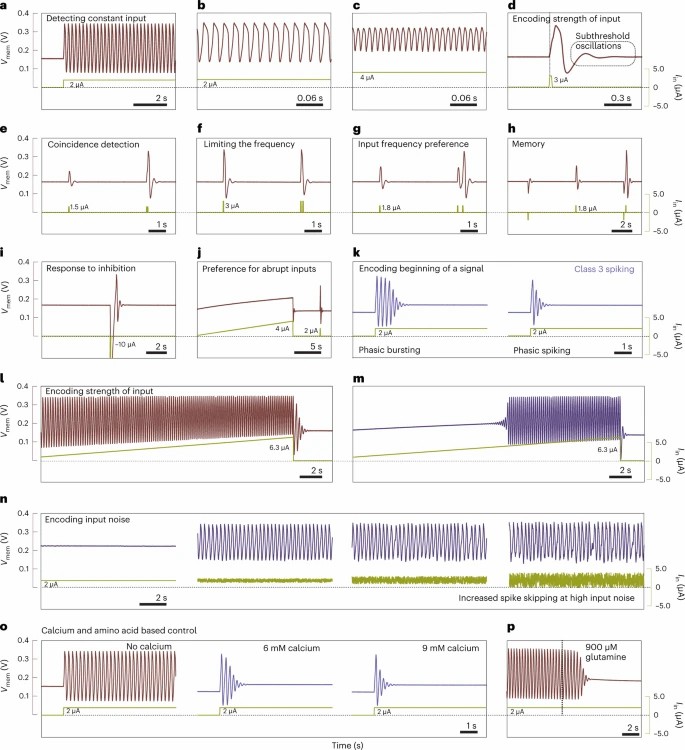
(a–p) 包括周期性尖峰 (a)、通过调节 \(R_{\text{dk}}\) 和 \(C_{\text{mem}}\) 实现的高频周期性尖峰 (b, c)、潜伏期 (d)、积分 (e)、不应期 (f)、共振 (g)、阈值变化 (h)、反弹尖峰 (i)、适应性 (j)、3 类尖峰——突发尖峰 (k)、1 类尖峰 (l)、2 类尖峰 (m)、带噪声输入的随机尖峰 (n)、基于钙的从 1 类到 3 类尖峰的调节 (o) 和通过氨基酸谷氨酰胺的尖峰调节 (p)。
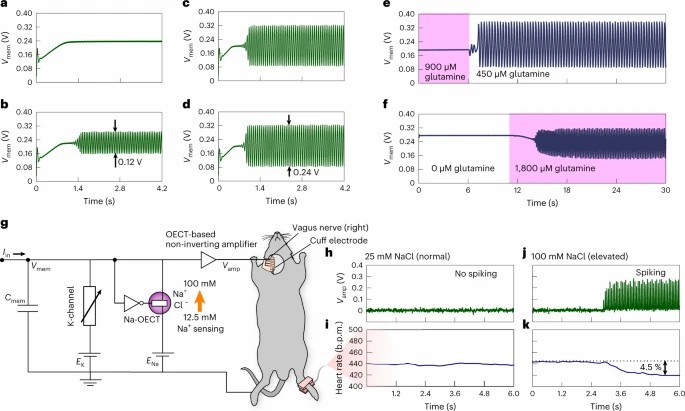
(a–d) 基于 NaCl 浓度 (12.5 mM (a), 25 mM (b), 50 mM (c), 和 100 mM (d)) 调节 c-OECN 的尖峰行为。 (e, f) 在低谷氨酰胺浓度 (<900 \(\mu\)M, e) 和高谷氨酰胺浓度 (>1,800 \(\mu\)M, f) 下的尖峰行为。 (g) c-OECN 电路通过 Na-OECT 检测 Na\(^+\) 离子,并通过 OECT 放大器和袖口电极集成到迷走神经中。 (h, i) 在低 NaCl 浓度 (25 mM, h) 下的放大器输出及相应的心率变化 (i)。 (j, k) 在高 NaCl 浓度 (100 mM, j) 下的放大器输出及相应的心率变化 (k)。
结论与展望
本研究开发的c-OECN展示了离子驱动的尖峰行为和高度生物相容的特性,为类生物电化学神经元的研究开辟了新路径。未来研究可探索其在复杂生物信号环境中的稳定性,并开发智能闭环系统,用于生物医学领域如炎症调控、代谢控制和脑机接口。
论文直达
原文标题:Ion-tunable antiambipolarity in mixed ion–electron conducting polymers enables biorealistic organic electrochemical neurons
原文卷期号:Nature Materials 2023, 22, 242–248
点击以下链接阅读原文:

