摘要

关键词
- 胰腺癌检测 (Pancreatic Cancer Detection)
- 非对比CT (Non-Contrast CT)
- 深度学习 (Deep Learning)
- 人工智能筛查 (AI Screening)
- 多中心验证 (Multicenter Validation)
- 早期癌症检测 (Early Cancer Detection)
- 大规模筛查 (Large-Scale Screening)
研究背景
胰腺导管腺癌(PDAC)是全球死亡率最高的恶性肿瘤之一,其晚期诊断导致治疗机会丧失,而早期检测可显著延长生存期。由于PDAC的低发病率和现有筛查方法的局限性,基于人工智能和非对比CT的低成本、大规模筛查具有重要意义。然而,非对比CT上胰腺病变的低对比度和复杂性使得人工识别具有挑战性。本研究开发的PANDA模型利用深度学习技术,结合高质量的训练数据和多中心验证,克服了非对比CT在胰腺癌检测中的技术瓶颈,为推动广泛临床应用铺平了道路。
创新点
- 开发了基于非对比CT的深度学习胰腺癌检测模型PANDA。
- 模型在多中心验证中表现出超越传统放射科医生的检测能力。
- 提供了无需对比增强剂的无创检测手段,降低了成本和风险。
- 模型具备实时应用潜力,适用于大规模人群筛查。
研究内容
本研究构建了PANDA模型,通过非对比CT实现胰腺病变的检测、分割和分类。模型分为三阶段:胰腺定位、病灶检测和差异化诊断。在3208例患者数据上训练,模型通过多中心(9个中心,5337例患者)和真实场景验证(20530例患者),展示了卓越的检测性能。
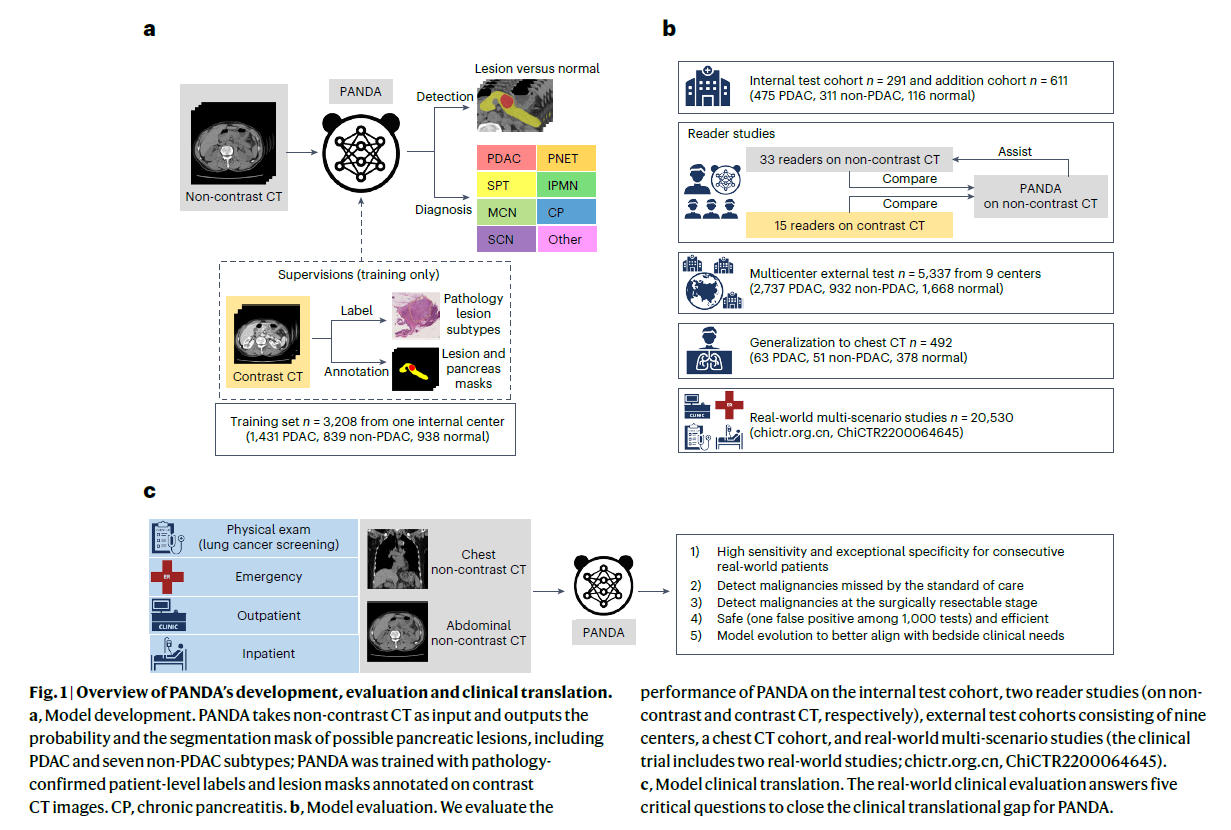
(a) 模型开发。PANDA以非增强CT作为输入,输出可能胰腺病变(包括PDAC和七种非PDAC亚型)的概率及分割掩码;PANDA通过病理确诊的患者标签和在增强CT图像上标注的病变掩码进行训练。CP,慢性胰腺炎。
(b) 模型评估。我们在内部测试队列、两项读者研究(分别基于非增强CT和增强CT)、外部多中心测试队列(包括9个中心)、胸部CT队列以及真实世界多场景研究中评估PANDA的性能。
(c) 模型的临床转化。通过真实世界的临床评估,PANDA回答了五个关键问题,旨在弥合临床转化中的差距。
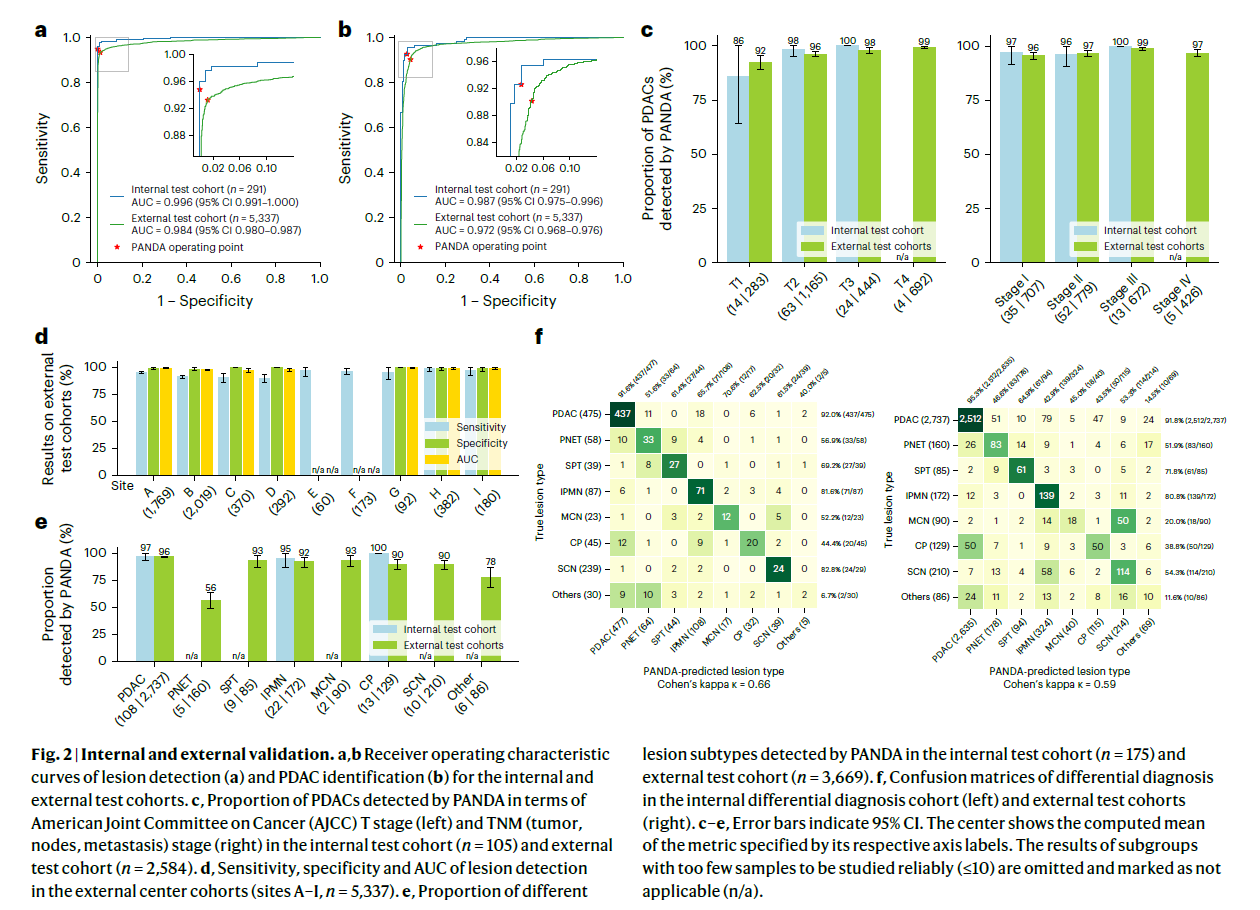
(a, b) 病变检测 (a) 和 PDAC识别 (b) 的受试者工作特征 (ROC) 曲线,基于内部和外部测试队列。
(c) PANDA在美国癌症联合委员会 (AJCC) T分期 (左) 和 TNM分期 (右) 中检测到PDAC的比例,涵盖内部测试队列(n = 105)和外部测试队列(n = 2,584)。
(d) 在外部中心队列(A至I,共5,337例)中病变检测的敏感性、特异性和AUC。
(e) PANDA在内部测试队列(n = 175)和外部测试队列(n = 3,669)中检测到不同病变亚型的比例。
(f) 在内部和外部测试队列中的差异诊断混淆矩阵,展示病理确认的病变类型的分类性能。
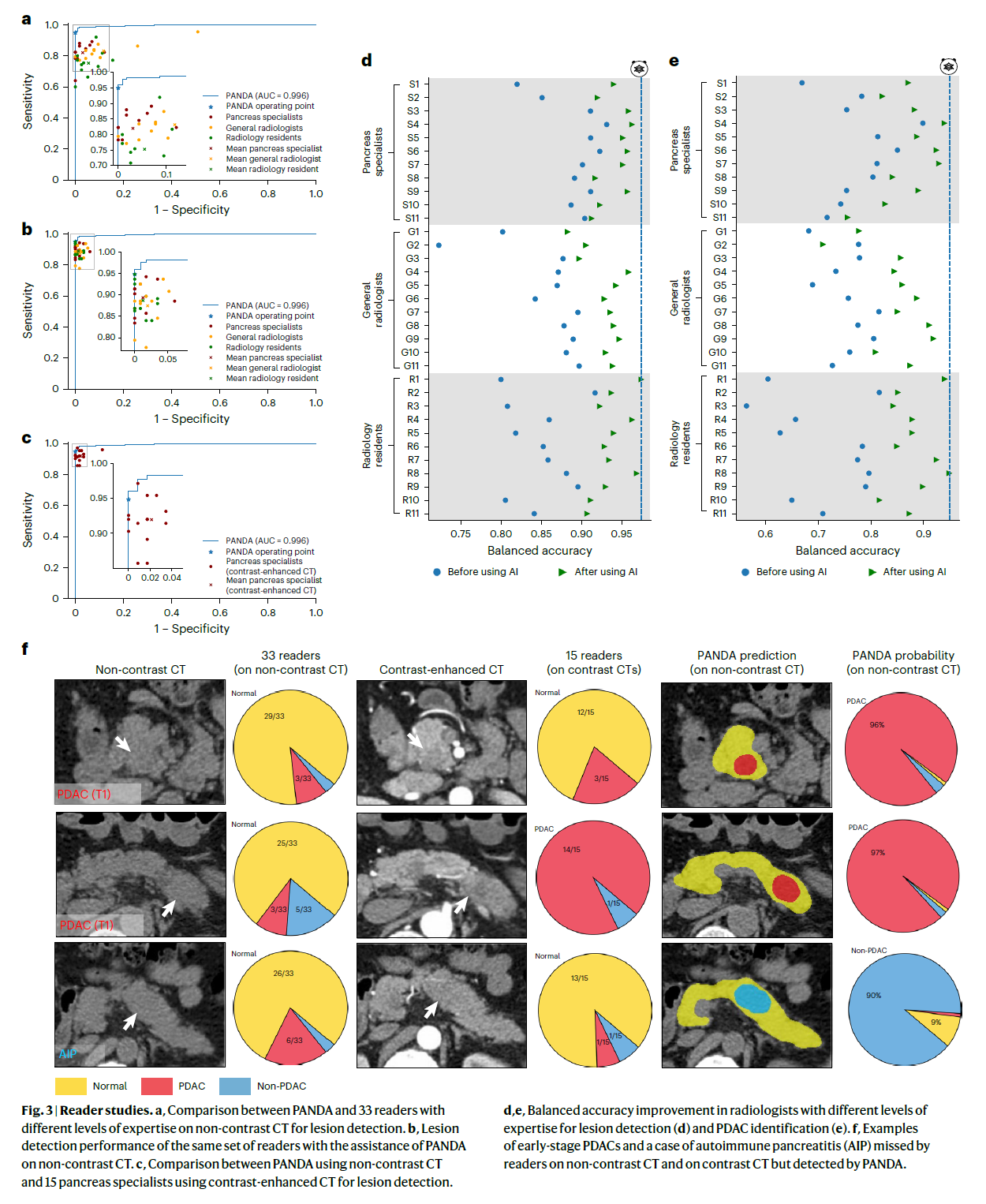
(a) 比较PANDA与33位不同专业水平的读者在非增强CT上的病变检测性能。
(b) 同一组读者在PANDA辅助下的病变检测性能改进。
(c) 比较PANDA在非增强CT上的性能与15位胰腺专家在增强CT上的性能。
(d, e) 不同专业水平的放射科医生在病变检测 (d) 和PDAC识别 (e) 上的平衡准确率改进。
(f) 示例:PANDA检测到的早期PDAC及自身免疫性胰腺炎(AIP)病例,而这些病例在非增强CT和增强CT中均被读者漏诊。
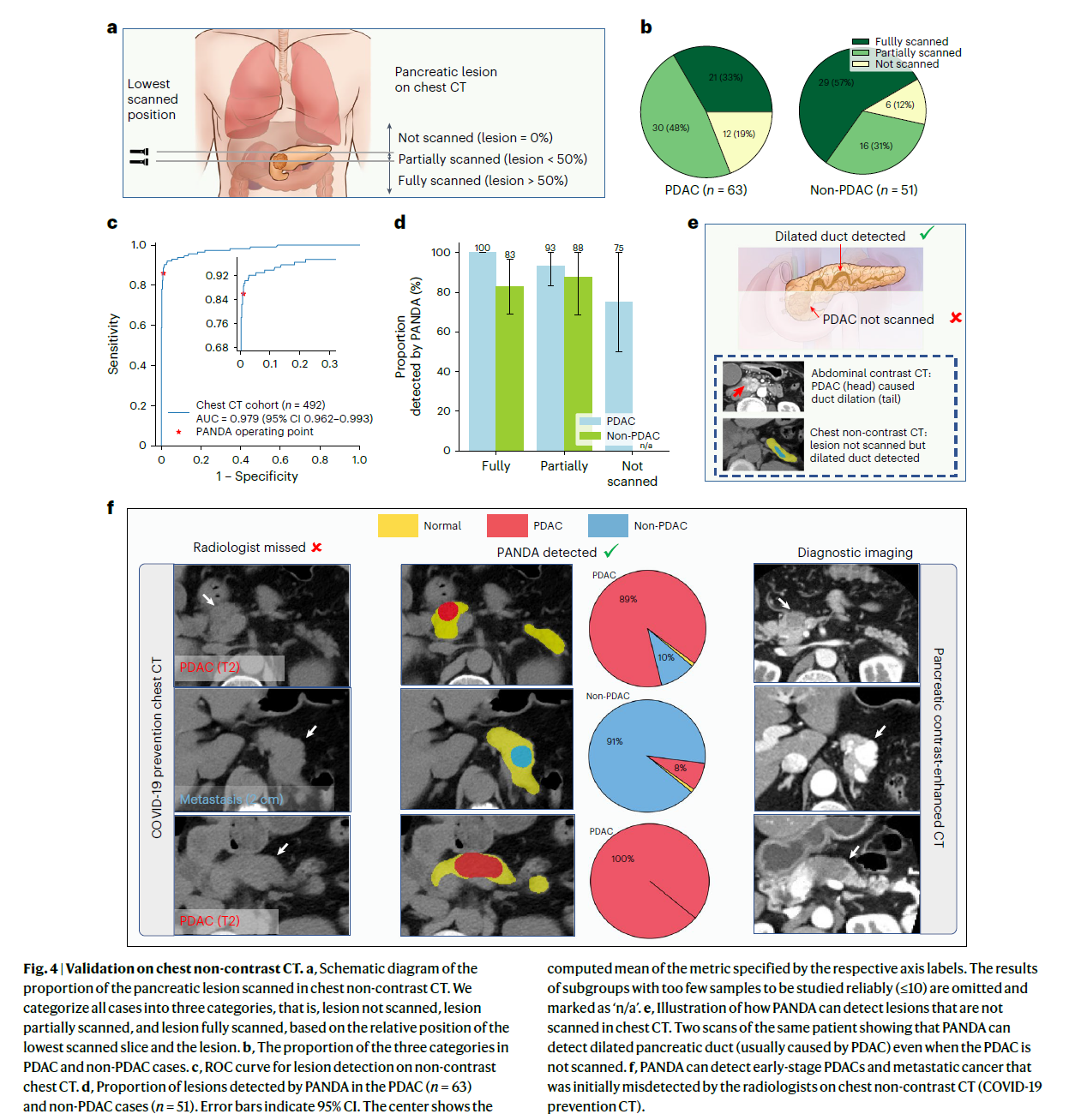
(a) 胸部非增强CT中胰腺病变扫描比例的示意图,病例被分为未扫描、部分扫描及完全扫描三类。
(b) 在PDAC (n = 63) 和非PDAC病例 (n = 51) 中,这三类扫描比例的分布。
(c) 胸部非增强CT上病变检测的ROC曲线。
(d) PANDA在PDAC和非PDAC病例中检测到的病变比例及其误差条显示的95%置信区间。
(e) 示例:PANDA如何检测未在胸部CT中扫描的病变(例如,通过检测胰管扩张)。
(f) PANDA检测到的早期PDAC及转移癌的示例,这些病例最初在胸部非增强CT中被放射科医生漏诊。
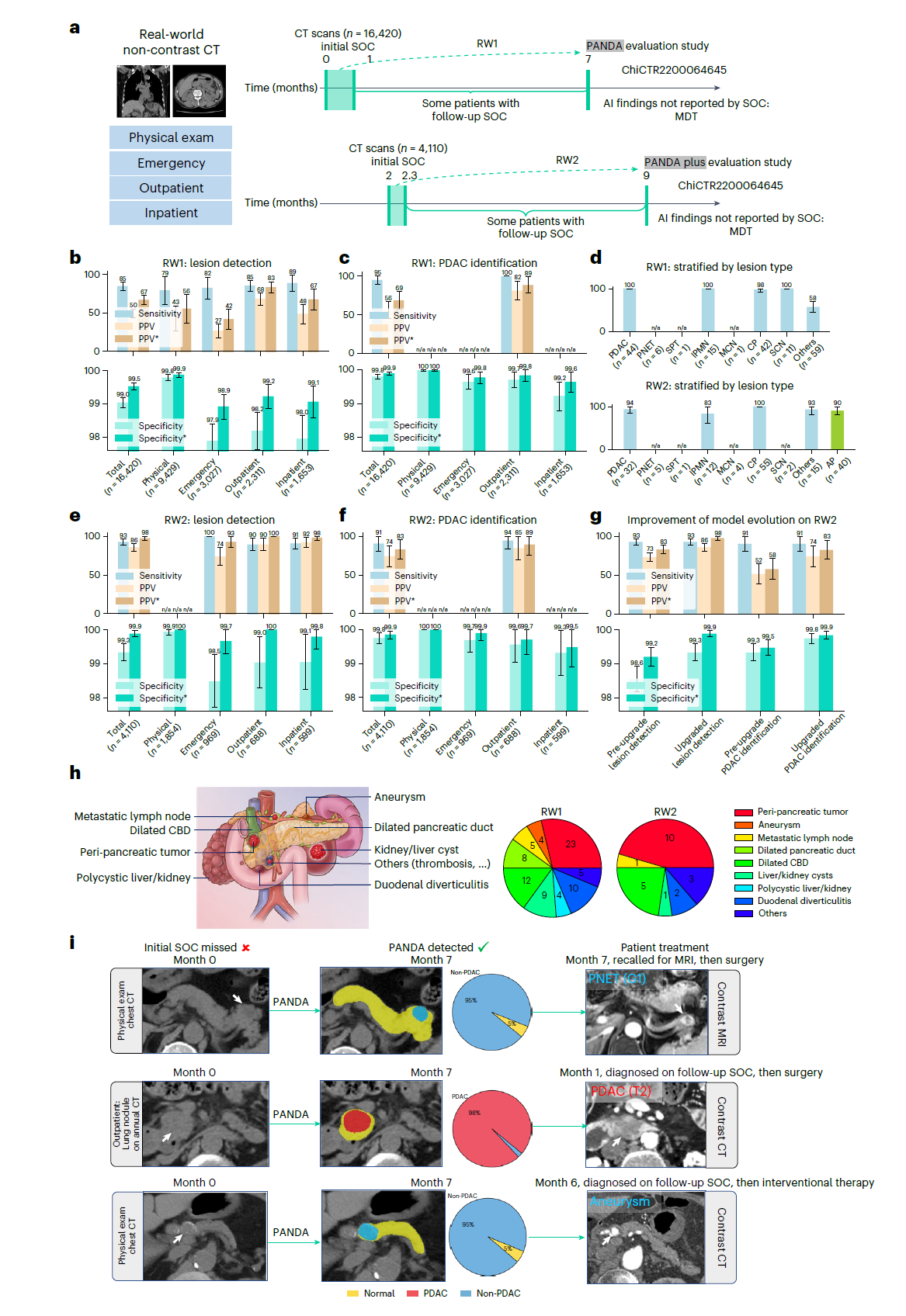
(a) PANDA和PANDA Plus模型的两轮真实世界评估数据收集流程。
(b, c, e, f) 在RW1 (n = 16,420) 和 RW2 (n = 4,110) 队列上的敏感性、特异性及阳性预测值 (PPV)。带*的指标表示排除(胰)胰腺相关发现后的调整结果。
(d) 在RW1 (n = 179) 和 RW2 (n = 166) 队列中不同病变类型的检测比例。
(g) PANDA和PANDA Plus在RW2队列 (n = 4,110) 上的性能对比。
(h) (胰)胰腺相关发现示例及其由PANDA检测到的数量。CBD,胆总管。
(i) PANDA检测到的由初始SOC漏诊的病例示例。
结论与展望
本文提出的PANDA模型在非对比CT上实现了胰腺病变的高效检测,为低成本、大规模的胰腺癌早期筛查提供了可能。未来研究将进一步优化模型的泛化性能,并在国际多中心数据上验证其普适性,以促进AI在医疗影像中的全面应用。
论文直达
原文标题:Large-Scale Pancreatic Cancer Detection via Non-Contrast CT and Deep Learning
Nat. Med., 2023, 29, 3033–3043.
点击以下链接阅读原文:

